Cutaneous infection caused by Mycobacterium abscessus in an immunocompetent patient: A diagnostic challenge
Dermatol Rev Mex. 2026; 70 (2): 318-321. https://doi.org/10.24245/dermatolrevmex.v70i2.10906
Erandy Alicia Salcedo Elguea,1 César Alexander Martínez Calderón,1 Nancy Gabriela Méndez Vizcarra2
1 Medicina Interna, Hospital General B, Instituto de Seguridad Social y Servicios Sociales de los Trabajadores del Estado (ISSSTE), Ciudad Juárez, Chihuahua, México.
2 Dermatos Skin Clinic, Ciudad Juárez, Chihuahua.
ANTECEDENTES
Las micobacterias no tuberculosas son microorganismos ambientales capaces de causar infecciones en humanos, principalmente en la piel y los tejidos blandos. En los últimos años, las infecciones por micobacterias de rápido crecimiento, como Mycobacterium abscessus, han adquirido mayor relevancia clínica debido a su resistencia antimicrobiana y a los retos diagnósticos que representan.1,2
Mycobacterium abscessus está ampliamente distribuida en el ambiente, particularmente en diversas fuentes de agua, lo que favorece la exposición humana.1 Aunque tradicionalmente se ha considerado un patógeno oportunista, se ha documentado su capacidad para causar infección activa en pacientes inmunocompetentes, especialmente tras exposiciones ambientales o procedimientos invasivos.1,3
Las infecciones cutáneas por M. abscessus suelen manifestarse con lesiones inespecíficas, como pápulas, nódulos, ulceras o abscesos que, con frecuencia, no responden a antibióticos convencionales, lo que retrasa el diagnóstico.4,5 En este contexto, las técnicas moleculares han cobrado relevancia al permitir una identificación rápida del agente etiológico y un tratamiento dirigido.5
Se comunica el caso de una paciente inmunocompetente con infección cutánea por Mycobacterium abscessus; destaca la importancia de considerar a las micobacterias no tuberculosas en el diagnóstico diferencial de lesiones cutáneas resistentes al tratamiento convencional.
CASO CLÍNICO
Paciente femenina de 15 años, previamente sana que, después de un viaje a Cancún, Quintana Roo, manifestó una dermatosis localizada en el talón del pie izquierdo (Figura 1A), con una lesión cupuliforme de base eritematosa y material blanquecino en su superficie, de 1 cm de diámetro, dolorosa a la palpación. Posteriormente manifestó una segunda lesión en la región maleolar externa del mismo pie, con características clínicas similares a la lesión inicial. Figura 1B
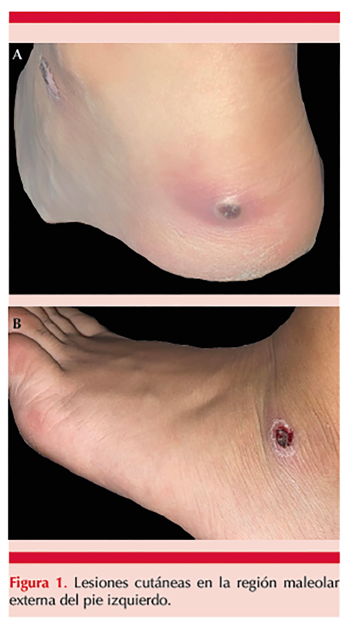
Acudió a valoración médica en consulta privada, donde recibió tratamiento con clindamicina y amoxicilina por vía oral, sin mejoría clínica; por el contrario, las lesiones evolucionaron y mostraron secreción purulenta.
Se tomó biopsia de las lesiones cutáneas, cuyo estudio histopatológico reportó dermatitis crónica granulomatosa con células gigantes tipo Langhans (Figura 2) y áreas de necrosis licuefactiva focal. La tinción de Grocott-Gomori fue negativa para hifas o esporas. La prueba cutánea con derivado proteico purificado (PPD) y la radiografía posteroanterior de tórax fueron negativas.
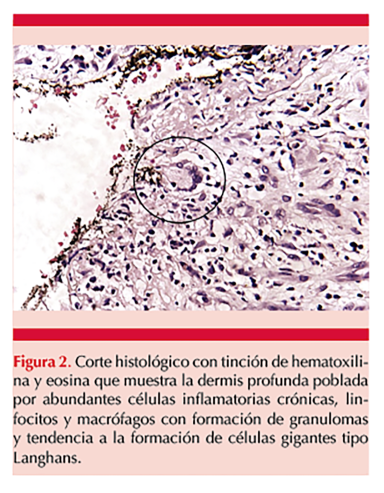
La muestra se envió para la realización de un ensayo de reacción en cadena de la polimerasa (PCR) para la detección de Mycobacterium avium, M. tuberculosis, M. abscessus, M. kansasii y M. simiae, entre otros, que resultó positiva para Mycobacterium abscessus.
Con base en estos hallazgos, se inició tratamiento con ciprofloxacino a dosis de 500 mg cada 12 horas durante un mes, con lo que se obtuvo alivio completo de las lesiones. En la consulta de seguimiento dos meses después del inicio del tratamiento no se documentaron recidivas.
DISCUSIÓN
Mycobacterium abscessus es una micobacteria no tuberculosa de rápido crecimiento cuya importancia clínica ha aumentado de manera significativa en las últimas décadas. Su clasificación taxonómica ha evolucionado hasta conformar el complejo M. abscessus, integrado por las subespecies abscessus, bolletii y massiliense, diferenciadas mediante análisis genómicos, lo que ha permitido comprender mejor su diversidad genética y su repercusión en la virulencia y la respuesta terapéutica.6
Este complejo está ampliamente distribuido en el ambiente, incluido el suelo, agua dulce y salada, sistemas de agua potable y dispositivos médicos.¹ Esta amplia distribución explica la elevada exposición humana. Aunque durante años se consideró un patógeno oportunista, en la actualidad se reconoce su capacidad para producir infección activa en pacientes inmunocompetentes, atribuida a diversos factores de virulencia.3
Entre los principales mecanismos patogénicos destaca su pared celular rica en lípidos, que favorece la formación de biopelículas, lo que facilita la supervivencia ambiental y la resistencia antimicrobiana al limitar la penetración de antibióticos y la acción del sistema inmunitario.2,7 Asimismo, su capacidad oligotrófica le permite tener mínimos requerimientos nutricionales y de fuentes de carbono, con lo que puede sobrevivir en ambientes hostiles, como sistemas de agua tratada, donde otros microorganismos no persisten.7
M. abscessus también tiene la capacidad de sobrevivir intracelularmente en macrófagos mediante la inhibición de la fusión fagosoma-lisosoma y la neutralización de radicales libres, procesos regulados por lípidos de la pared celular, como los glicopeptidolípidos.8 La transición del morfotipo liso al rugoso, asociada a la pérdida de estos glicopeptidolípidos, se relaciona con mayor virulencia, inflamación tisular y peor evolución clínica.8 Además, el sistema de secreción ESX-4 contribuye a la supervivencia intracelular al bloquear la acidificación fagosomal y facilitar la disrupción de la membrana del fagosoma, lo que facilita la replicación intracelular del patógeno.9
Desde el punto de vista clínico, el complejo M. abscessus puede causar infecciones cutáneas, pulmonares y, con menor frecuencia, del sistema nervioso central.5 Las infecciones cutáneas suelen adquirirse por contacto directo con agua o material contaminado a través de traumatismos, procedimientos quirúrgicos o exposiciones ambientales, y se manifiestan con lesiones inespecíficas, como pápulas, nódulos, pústulas, úlceras o abscesos.4,5
En términos histopatológicos, las lesiones muestran inflamación granulomatosa supurativa con infiltrados mixtos y ocasional necrosis, hallazgos que no son patognomónicos y pueden observarse en otras infecciones crónicas.5,10 Por ello, el diagnóstico representa un reto y requiere un enfoque multimodal que integre datos clínicos, histológicos, microbiológicos y moleculares.5 Si bien el cultivo sigue siendo el patrón de referencia, su rendimiento limitado y el tiempo prolongado de incubación hacen que las técnicas moleculares, como la PCR dirigida a genes específicos (16S rRNA, rpoB, hsp65), sean métodos fundamentales para una identificación rápida y precisa.1,5
El tratamiento de la infección por M. abscessus es complejo debido a su resistencia intrínseca y adquirida a múltiples antibióticos, relacionada con la baja permeabilidad de su pared celular, sistemas de expulsión, producción de β-lactamasas y la expresión del gen erm(41), responsable de la resistencia inducible a macrólidos.1,2,11 Si bien se recomiendan esquemas combinados y prolongados, la respuesta clínica es variable. En infecciones cutáneas localizadas en pacientes inmunocompetentes, el tratamiento oral puede ser suficiente, como se evidenció en la paciente del caso.
CONCLUSIONES
La infección cutánea por Mycobacterium abscessus es un padecimiento poco frecuente pero clínicamente relevante, cuyo diagnóstico suele ser difícil debido a la inespecificidad de sus manifestaciones y a la falta de respuesta a antibióticos convencionales. Aunque tradicionalmente se ha considerado un patógeno oportunista, puede causar enfermedad significativa, incluso en pacientes inmunocompetentes. La heterogeneidad del cuadro clínico y la limitada sensibilidad de los métodos diagnósticos convencionales resaltan la importancia de mantener un alto índice de sospecha, particularmente en el contexto de exposición ambiental. El diagnóstico oportuno mediante técnicas moleculares y el inicio temprano de un tratamiento dirigido son determinantes para una evolución favorable y para evitar complicaciones y recurrencias.1,5,12
REFERENCIAS
1. Victoria L, Gupta A, Goméz JK, Robledo J. Mycobacterium abscessus complex: A review of recent developments in an emerging pathogen. Fron Cell Infect Microbiol 2021; 11: 659997. https://doi.org/10.3389/fcimb.2021.659997
2. Nessar R, Cambau E, Reyrat JM, et al. Mycobacterium abscessus: A new antibiotic nightmare. J Antimicrob Chemother 2012; 67 (4): 810-8. https://doi.org/10.1093/jac/dkr578
3. Ferrell KC, Johansen MD, Triccas JA, Counoupas C. Virulence mechanisms of Mycobacterium abscessus: Current knowledge and implications for vaccine design. Front Microbiol 2022; 13: 842017. https://doi.org/10.3389/fmicb.2022.842017
4. Kothavade RJ, Dhurat RS, Mishra SN, Kothavade UR. Clinical and laboratory aspects of the diagnosis and management of cutaneous and subcutaneous infections caused by rapidly growing mycobacteria. Eur J Clin Microbiol Infect Dis 2013; 32 (2): 161-88. https://doi.org/10.1007/s10096-012-1766-8
5. Mehta N, Tyagi M, Ramam M, Khaitan BK. Cutaneous atypical Mycobacterial infections: A brief review. Indian Dermatol Online J 2024; 15 (6): 909-19. https://doi.org/10.4103/idoj.idoj_838_23
6. Bryant JM, Grogono DM, Greaves D, Forewaker J. Whole-genome sequencing to identify transmission of Mycobacterium abscessus between patients with cystic fibrosis: A retrospective cohort study. Lancet 2013; 381 (9877): 1551-60. https://doi.org/10.1016/S0140-6736(13)606327
7. Falkinham JO. Impact of human activities on the ecology of nontuberculous mycobacteria. Future Microbiol 2010; 5 (6): 951-60. https://doi.org/10.2217/fmb.10.53
8. Gutiérrez AV, Viljoen A, Ghigo E, et al. Glycopeptidolipids, a double-edged sword of the Mycobacterium abscessus complex. Front Microbiol 2018; 9: 1145. https://doi.org/10.3389/fmicb.2018.01145
9. Laencina L, Dubois V, Le Moigne V, Viljoen A. Identification of genes required for Mycobacterium abscessus growth in vivo with a prominent role of the ESX-4 locus. Proc Natl Acad Sci USA 2018; 115 (5): 1002-11. https://doi.org/10.1073/pnas.1713195115
10. Bartralot R, Pujol RM, García-Patos V, et al. Cutaneous infections due to nontuberculous mycobacteria: histopathological review of 28 cases. Comparative study between lesions observed in immunosuppressed patients and normal hosts. J Cutan Pathol 2000; 27 (3): 124-9. https://doi.org/10.1034/j.1600-0560.2000.027003124.x
11. Story-Roller E, Maggioncalda EC, Cohen KA, Lamichhane G. Mycobacterium abscessus and β-lactams: Emerging insights and potential opportunities. Front Microbiol 2018; 9: 2273. https://doi.org/10.3389/fmicb.2018.02273
12. Fujishima C, Tahara J, Munemoto S, et al. Cutaneous nontuberculous mycobacterial infections in Japan: Review of the Japanese literature. J Dermatol 2022; 49 (11): 1075-84. https://doi.org/10.1111/1346-8138.16531
ORCID
https://orcid.org/0009-0004-0171-3464
https://orcid.org/0009-0008-5099-7941
https://orcid.org/0009-0002-2707-5335
Recibido: enero 2026
Aceptado: enero 2026
Este artículo debe citarse como: Salcedo-Elguea EA, Martínez-Calderón CA, Méndez-Vizcarra NG. Infección cutánea por Mycobacterium abscessus en una paciente inmunocompetente: un reto diagnóstico. Dermatol Rev Mex 2026; 70 (2): 318-321.

