Relapse of bullous pemphigoid after attenuated virus vaccine against COVID-19 application.
Dermatol Rev Mex. 2021; 65 (6): 1017-1020. https://doi.org/10.24245/dermatolrevmex.v65i6.7179
Ana Isabel Macías-Macías,1 Osvaldo Gabriel Saavedra-Casas,2 Moisés Humberto Capilla-García,3 Adameck Abraham Hernández-Collazo4
1 Residente de Medicina Interna, Hospital General ISSSTE Aguascalientes, Aguascalientes, México.
2 Residente de Medicina Interna, Hospital General de Zona núm. 11, IMSS, Nuevo Laredo, Tamaulipas, México.
3 Estudiante de Medicina, Universidad Autónoma de Aguascalientes, Aguascalientes, México.
4 Dermatólogo, Nuevo Hospital Miguel Hidalgo, Aguascalientes, México.
Estimados editores:
El penfigoide bulloso es una enfermedad ampollosa autoinmunitaria caracterizada por autoanticuerpos IgG circulantes contra antígenos de hemidesmosomas de la zona de la membrana basal: las proteínas BP180 y BP230.1 Existen muchos factores desencadenantes conocidos de este trastorno inmunobulloso, como son: la radiación ultravioleta (UV), fármacos, traumatismos y quemaduras.1 También se ha documentado que algunas inmunizaciones, como la vacuna contra la difteria, tos ferina, rabia y poliomielitis, pueden desencadenar la aparición de penfigoide ampolloso; sin embargo, su mecanismo aún no está definido.2 Comunicamos un caso de recaída de PB posterior a la aplicación de vacunas de virus atenuados contra COVID-19.
CASO CLÍNICO
Paciente masculino de 90 años de edad con diagnósticos de hipertensión arterial sistémica en tratamiento con felodipino, enfermedad pulmonar obstructiva crónica en tratamiento sintomático con bromuro de ipatropio y ejercicios respiratorios con inspirómetro incentivo, aumento de automatismo supraventricular y ventricular en tratamiento con amiodarona y edema periférico, sin cambio en la terapéutica desde septiembre de 2020. Tenía el antecedente conocido de penfigoide bulloso (anticuerpos anti-beta 2 glicoproteína negativos) desde los 87 años de edad confirmado por inmunofluorescencia directa que remitió al suspender la administración de furosemida, propranolol y espironolactona; enfermedad que se mantuvo en control sólo con cuidados generales de la piel desde entonces y evitando el reinicio de esos fármacos. Acudió por manifestar ronchas y prurito en la espalda y los muslos que luego desarrollaron ampollas un día después de la aplicación de vacuna de virus atenuados contra SARS-CoV-2: Sinovac.
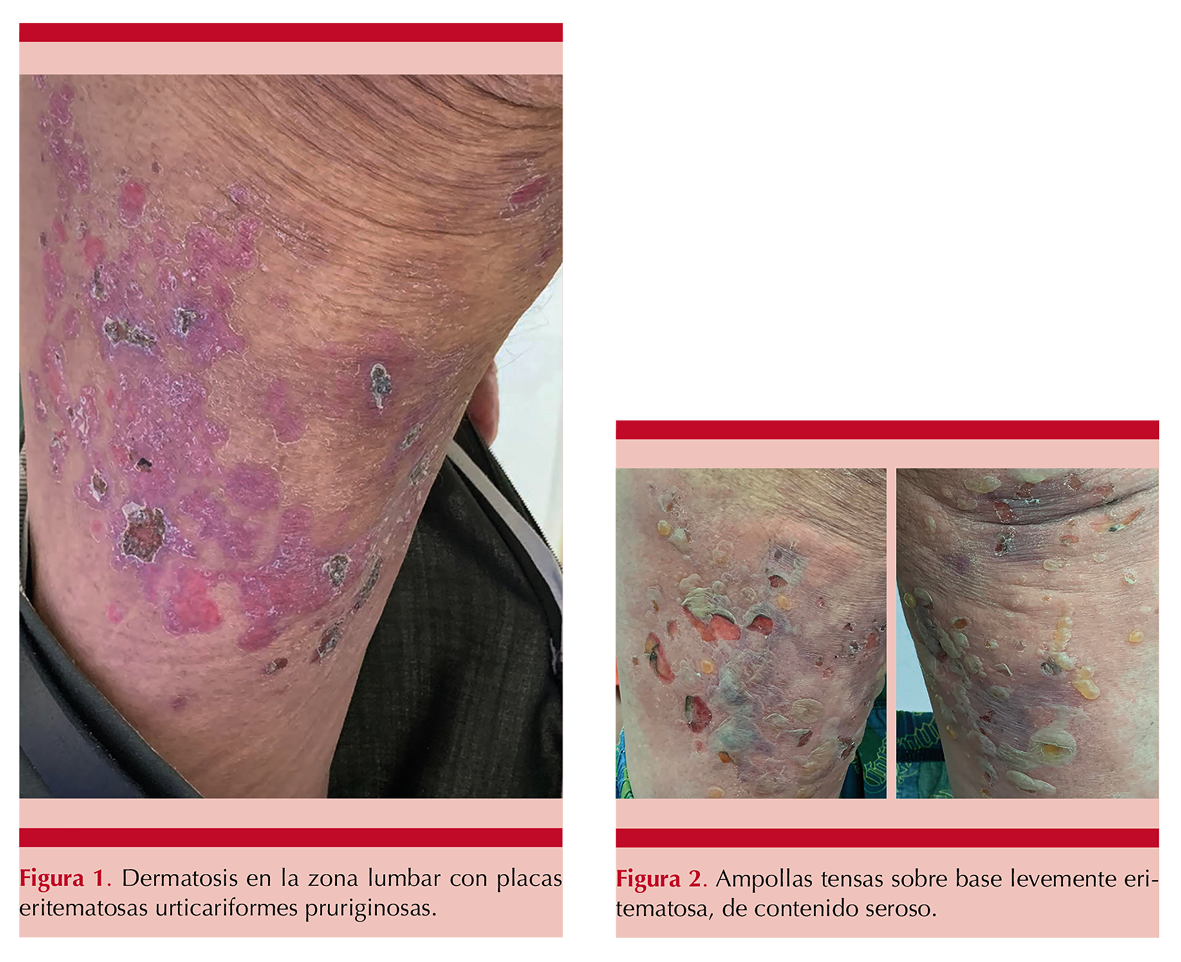
A la exploración se encontraron en la zona lumbar múltiples placas eritematosas y urticariformes (Figura 1) y en la cara posterior de los muslos bullas tensas de dimensiones no mayores a 4 cm que tendían a confluir, algunas ya erosionadas (Figura 2). El estudio histopatológico del borde de una lesión ampollosa reveló una ampolla subepidérmica con infiltrado perivascular de linfocitos y eosinófilos sugerente de penfigoide bulloso (Figura 3). Se inició tratamiento con prednisona a dosis de 0.75 mg/kg, minociclina 50 mg/día, nicotinamida 250 mg dos veces al día y propionato de clobetasol tópico con alivio evidente de los síntomas y desaparición de las lesiones a partir del quinto día de tratamiento. Figura 4

DISCUSIÓN
El penfigoide bulloso es un trastorno inmunobulloso con formación de autoanticuerpos dirigidos contra los hemidesmosomas BP230 y principalmente la zona no colágena (NC16A) de la proteína transmembranal BP180.3 Existen numerosos desencadenantes de la enfermedad, que incluyen radiación ultravioleta, fármacos (principlamente antihipertensivos y diuréticos), traumatismos, radioterapia y quemaduras.1 El desencadenante es capaz de activar una respuesta inmunitaria mediada por células B que activan el complemento vía autoanticuerpos liberando proteasas que ocasionan escisión subepidérmica.3 Se han implicado algunas vacunas como desencadenantes del penfigoide bulloso, que incluyen la vacuna contra tétanos, difteria y tos ferina (Tdap), vacuna contra la enfermedad de Haemophilus influenzae tipo B, hepatitis B, neumococo, influenza porcina y rabia (Cuadro 1).2 El periodo entre la administración de vacunas y la aparición de las lesiones es variable y puede ser de un día a un mes.2 El mecanismo por el cual se induce la enfermedad en respuesta a la vacuna aún no se conoce, pero se ha propuesto como desencadenante la exposición a virus atenuados que estimula la inmunidad humoral con posterior liberación masiva de anticuerpos, activación de células Th17 con liberación de IL-17 o deficiencia de CD25 posterior a la inmunización.2,3,4 La vacuna producida por Sinovac Life Siencies (Beijin), conocida como CoronaVac, contiene un virión SARS-CoV-2 íntegro propagado en células Vero e inactivado con b-propiolactona con coadyuvante de hidróxido de aluminio, es administrada vía intramuscular en dos dosis: día 0 y día 14-28.5 Las vacunas con virus atenuados se incorporan de coadyuvantes (QS21, AS01, MF59 o hidróxido de aluminio), que tienen una función proinflamatoria a través de inducir anticuerpos con múltiples epítopos con unión mejorada a C1q, los cuales podrían ser capaces de activar las proteasas causantes de las ampollas de penfigoide bulloso en pacientes predispuestos.3,6

La asociación temporal entre la administración de la vacuna y la aparición de lesiones ampollosas fue un indicador de que la vacuna con virus atenuados contra COVID-19 podría ser el desencadenante de la recaída en un paciente predispuesto. Debido a la terapéutica con esteroide sistémico y el alto riesgo de recaída se postergó la segunda dosis de vacuna o se propuso cambio de mecanismo de inmunización.
REFERENCIAS
1. Genovese G, Di Zenzo G, Cozzani E, Berti E, Cugno M, Marzano AV. New insights into the pathogenesis of bullous pemphigoid: 2019 update. Front Immunol 2019; 10: 1506. doi: 10.3389/fimmu.2019.01506.
2. Maki N, Hashimoto T, Yamada T, Ishii N, Tsuruta D, Demitsu T. Case of pemphigoid with immunoglobulin G antibodies to BP180 C-terminal domain and laminin-γ1 (p200) developed after pneumococcal vaccination. J Dermatol 2021; 48: 101-105. doi: 10.1111/1346-8138.15626.
3. Cao T, Shao S, Fang H, Li B, Wang G. Role of regulatory immune cells and molecules in autoimmune bullous dermatoses. Front Immunol 2019; 10: 1746. doi: 10.3389/fimmu.2019.01746.
4. Baroero L, Coppo P, Bertolino L, Maccario S, Savino F. Three case reports of post immunization and post viral Bullous Pemphigoid: looking for the right trigger. BMC Pediatrics 2017; 17: 1-5. doi: 10.1186/s12887-017-0813-0.
5. Palacios R, Patiño EG, de Oliveira Piorelli R, Conde M, Batista P, Zeng G et al. Double-blind, randomized, placebo-controlled phase III clinical trial to evaluate the efficacy and safety of treating healthcare professionals with the adsorbed COVID-19 (inactivated) vaccine manufactured by Sinovac–PROFISCOV: A structured summary of a study protocol for a randomised controlled trial. Trials 2020; 21: 1-3. doi: 10.1186/s13063-020-04775-4.
6. Kurtovic L., Beeson JG. Complement factors in COVID-19 therapeutics and vaccines. Trends Immunol 2021; 42: 94-103. doi: 10.1016/j.it.2020.12.002.
Recibido: septiembre 2021
Aceptado: octubre 2021
Este artículo debe citarse como: Macías-Macías AI, Saavedra-Casas OG, Capilla-García MH, Hernández-Collazo AA. Recaída de penfigoide ampolloso posterior a la aplicación de la vacuna de virus atenuados contra COVID-19. Dermatol Rev Mex 2021; 65 (6): 1017-1020.

